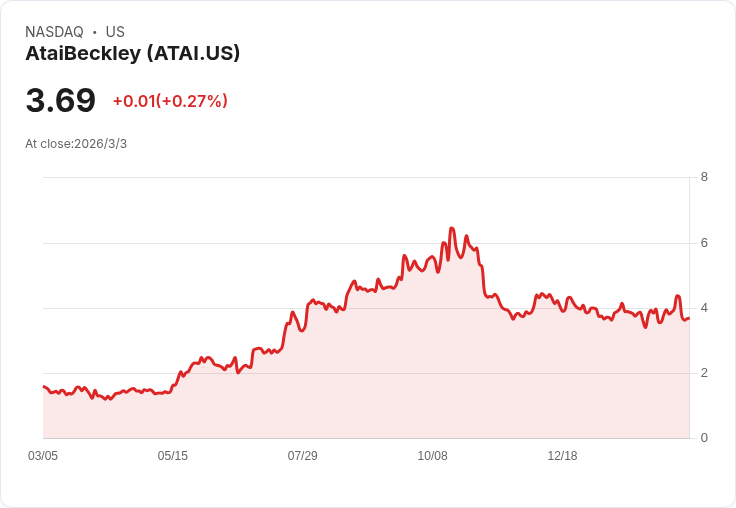
AtaiBeckley宣佈與FDA成功會議,將於2026年第二季啟動BPL-003的第三期臨床試驗,針對治療抗藥性憂鬱症。
AtaiBeckley Inc.(NASDAQ: ATAI)近日公告,其在與美國食品藥品監督管理局(FDA)的結束第二階段會議中獲得正面反饋,計劃於2026年第二季啟動BPL-003的第三期臨床試驗。該產品是一種專有的鼻用mebufotenin benzoate配方,旨在治療治療抗藥性憂鬱症(TRD)。FDA對此專案表示支援,並提供了關於設計和安全資料庫要求的建議。
這一里程碑事件緊隨著2025年底授予的突破性療法認證。即將展開的第三期計畫將包括兩個平行的關鍵研究——ReConnection 1和ReConnection 2,以及為期52週的開放標籤延伸研究,以評估長期安全性及個別再治療需求。其中,ReConnection 1將比較8毫克和4毫克單次劑量與安慰劑的效果,而ReConnection 2則將探索第1天和第15天的雙劑量誘導模式。
BPL-003的設計考慮到現有介入精神病學工作流程,預計能夠提供快速且持久的治療選擇,患者只需每年接受幾次治療,整體診所經歷約為兩小時。雖然AtaiBeckley被視為潛在投資機會,但一些分析師指出,某些人工智慧股票可能提供更大的上漲潛力和較低的下行風險。因此,未來市場走向值得密切關注。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌