
《鬼道》致富:美時在505(b)2領域的佈局→一本萬利!
第一代的高磷酸血症用藥FDA已核准的藥商有6種!其中以Sanofi的Sevelamer Carbonate(Renvela)市佔最高,其次為Takeda的Lanthanum Carbonate(Fosrenol咀嚼錠)!
整個高磷酸血症用藥市場,美國10E美、全球25E美!
儘管有6種FDA批准的磷酸鹽結合劑可供使用,但是估計75%的美國透析患者的高磷酸血症仍未得到控制,仍有未被滿足的需求。
在愛滋病、糖尿病和充血性心臟衰竭等各種慢性疾病中,維持透析患者的每日藥物負擔是最高的。一位病人平均每天要吃19粒(中位數)、49%的藥丸負荷來自磷酸鹽結合劑、較高的藥物負擔通常就代表較低的生活品質 (HR-QOL)、62%的患者醫囑遵從性差(自我報告),所以使用磷酸鹽結合劑治療高磷酸血症,仍有未被滿足的需求。
UNCYCIVE透過其專有的奈米顆粒技術,利用Lanthanum已知的磷酸鹽結合效力,來減少患者為控制高磷酸血症而必須服用的藥丸的數量和大小!


《鬼道》致富:美時在505(b)2領域的佈局→一本萬利!
第一代的高磷酸血症用藥FDA已核准的藥商有6種!其中以Sanofi的Sevelamer Carbonate(Renvela)市佔最高,其次為Takeda的Lanthanum Carbonate(Fosrenol咀嚼錠)!
整個高磷酸血症用藥市場,美國10E美、全球25E美!
儘管有6種FDA批准的磷酸鹽結合劑可供使用,但是估計75%的美國透析患者的高磷酸血症仍未得到控制,仍有未被滿足的需求。
在愛滋病、糖尿病和充血性心臟衰竭等各種慢性疾病中,維持透析患者的每日藥物負擔是最高的。一位病人平均每天要吃19粒(中位數)、49%的藥丸負荷來自磷酸鹽結合劑、較高的藥物負擔通常就代表較低的生活品質 (HR-QOL)、62%的患者醫囑遵從性差(自我報告),所以使用磷酸鹽結合劑治療高磷酸血症,仍有未被滿足的需求。
UNCYCIVE透過其專有的奈米顆粒技術,利用Lanthanum已知的磷酸鹽結合效力,來減少患者為控制高磷酸血症而必須服用的藥丸的數量和大小!

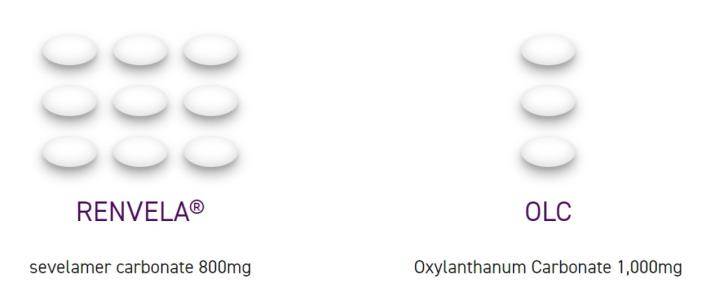
*Renvela 和 Fosrenol的平均每日劑量9顆
*Renazorb的平均每日劑量只要3顆,而且不需要咀嚼,直接以水吞服就好!
2023/10/23與FDA的Type C meeting中,FDA已同意Unicycive再做一個60位病人的開放標籤、單臂、多中心、多劑量關鍵臨床試驗。
該研究旨在評估耐受性和停藥事件發生率;因此,不需要再進行統計分析來證明功效,不需要其他臨床研究!
2023/12/18
Unicycive Therapeutics, Inc.宣布第一位患者已正式收案,預計在2024年第二季就會有top line data,之後就會送NDA申請!
所以,Unicycive拿到Renazorb的NDA藥證,幾乎已是板上釘釘的事,若無補件2025Q2前就會拿到藥證,接著美時申請韓國藥證也差不多就是一年左右,預估2026 Renazorb就可以貢獻美時營收!
雖然還有兩年多才貢獻營收,美時急嗎?美時缺錢嗎?美時缺藥嗎?美時缺市場嗎?→都不缺呀!美時不是新藥公司呀!他沒有風險呀!
美時是從「路邊攤」做到「連鎖餐飲企業」的營收王呀!美時是「通路王」呀!
欣賞一下,以下
三篇Unicycive的公告看進度
1. UNICYCIVE 宣布與 LOTUS 就 RENAZORB 在韓國達成獨家許可和開發協議
在新市場為高磷酸血症患者開發Renazorb的機會,協議包括預付款、特許權使用費和里程碑付款
2023/02/02
Unicycive宣布已與全球領先的製藥公司LOTUS(蓮花製藥)簽訂獨家協議,在韓國開發和商業化Renazorb。Renazorb是Unicycive的新型磷酸鹽結合劑,正在開發用於治療慢性腎病 (CKD) 患者的高磷血症。
Unicycive 首席執行官Shalabh Gupta 醫學博士說:「我們特別高興地宣布Renazorb 在亞洲的第二次合作,並很高興與全球知名製藥領導者Lotus合作。我們相信此次合作為Renazorb在韓國市場的進一步開發和商業化提供了最佳的基礎設施。高磷血症仍然是世界各地終末期腎病患者的一個嚴重問題,特別是因為目前可用的磷酸鹽結合劑的遵從性具有挑戰性。仍然需要一種新的治療方法,來提升患者的遵從性,例如 Renazorb。在 Unicycive,我們的主要目標之一是將 Renazorb 帶給世界各地的高磷血症患者,這一最新的合作夥伴關係強調了我們對這項使命的承諾。我們將繼續推進與其他關鍵地區潛在合作夥伴的討論,並期待我們在亞洲發起的全球合作夥伴關係的基礎上再接再厲。」
Lotus 執行長 Petar Vazharov 說:「與 Unicycive 的合作證明了我們為慢性病患者帶來新的治療選擇的努力。腎臟病是Lotus的重點治療領域之一,Lotus集團旗下的Alvogen韓國公司一直佔據主導地位,並以其他重磅產品為腎病市場做出了貢獻,例如用於CKD治療的Epoetin,其市場份額領先45%(根據 2022Q3 IQVIA資料)。Renazorb預計將為韓國 CKD 患者提供另一個高價值的臨床益處。」
根據協議條款,Lotus 將負責 Renazorb 在韓國的開發、註冊備案和批准。 此外,Lotus將全權負責從Unicycive進口該藥品以及Renazorb在韓國的商業化費用。 Unicycive 將獲得75萬美元的預付款,並在實現預先指定的監管和商業成就後可能獲得高達445萬美元的里程碑付款和分級特許權使用費。
2. UNICYCIVE Therapeutics與FDA就Oxylanthanum Carbonate (Renazorb, OLC) 提交新藥申請達成協議
2023/10/23
Unicycive Therapeutics, Inc.宣布該公司已與美國食品和藥物管理本局(FDA) 達成協議,關於Oxylanthanum Carbonate (Renazorb, OLC)的下一步以及提交新藥申請的整體要求。據6月報道,在與 FDA共享的新藥申請前一攬子計劃中,FDA 要求提供患者臨床數據以繼續進行備案。最近,在與 FDA 舉行的Type C 會議上,公司和FDA就提交NDA 的總體資料要求達成了協議,包括臨床數據、臨床前數據和CMC(化學、製造和品管)。
提醒一下,Unicycive打算利用505(b)(2)監管途徑提交(Renazorb, OLC)NDA,以引用目前批准的藥物Fosrenol。在Type C會議上,FDA 確認了關鍵臨床試驗的計畫。FDA同意該公司對60名參與者的研究設計,一旦參與者滴定至臨床有效劑量,將對60名參與者進行為期4週的(Renazorb, OLC)評估。
該研究旨在評估耐受性和停藥事件發生率;因此,不需要進行統計分析來證明功效,不需要其他臨床研究。我們相信,這項關鍵試驗的結果將增強我們臨床前研究的安全性資料包,而功效數據參考了Unicycive先前揭露的生物等效性(BE)研究。
Unicycive 執行長 Shalabh Gupta 醫學博士表示:「透過與FDA密切合作,我們清楚地了解了提交完整NDA資料包以獲得OLC潛在批准的要求。與FDA的一致性包括我們計劃的NDA套件的所有要素,包括臨床、臨床前和CMC要求。我們預計在今年年底前啟動OLC的關鍵試驗,預計在2024年第二季度獲得top line data。一旦完成試驗,我們計劃最終確定NDA所有資料並向FDA提交。」
截至2023年6月30日,Unicycive的現金狀況據報道為1,880 萬美元,預計將持續到2024年下半年,包括啟動和完成關鍵臨床試驗的能力。計劃中的臨床試驗預計將是一項開放標籤、單組、多中心、多劑量研究,旨在評估臨床有效劑量的 OLC對接受透析的慢性腎臟病 (CKD) 參與者的耐受性。
提醒一下,所有核准的磷酸鹽結合劑(包括 Fosrenol)均根據血清磷酸鹽控制按照劑量滴定方案給予患者。在Unicycive的臨床試驗中,一旦參與者滴定至臨床有效劑量且血清磷酸鹽範圍≤5.5 mg/dL,他們將接受為期4週的治療以評估血清磷酸鹽水平。
3. Unicycive Therapeutics 宣佈在慢性腎臟病透析患者的Oxylanthanum Carbonate (Renazorb, OLC)關鍵臨床試驗中招募首位患者
研究將對60名參與者進行評估,預計在2024年第二季得出結果
2023/12/18
Unicycive Therapeutics, Inc.宣布第一位患者入組其開放標籤、單臂、多中心、多劑量關鍵臨床試驗Oxylanthanum Carbonate (Renazorb, OLC)。OLC是第二代以lanthanum為基礎的磷酸鹽結合劑,採用專有的奈米顆粒技術,用於治療慢性腎臟病 (CKD) 透析患者的高磷血症。
首席執行官 Shalabh Gupta 醫學博士說:「在我們的(Renazorb, OLC)關鍵臨床試驗中啟動患者入組是一個重要的里程碑,因為我們努力減輕慢性腎臟病透析患者的服藥負擔並提高生活質量,OLC的新穎特性有可能使其成為價值數十億美元的高磷血症市場中同類最佳的磷酸鹽結合劑。這項關鍵試驗的數據是完成我們提交新藥申請NDA)所有資料的最後一個主要組成部分,將為醫生考慮為患者提供新的潛在療法時提供資訊。我們預計將在2024年第二季度報告試驗數據,並隨後不久提交NDA。」
研究的主要終點將評估臨床有效劑量的OLC對透析CKD患者的耐受性。次要終點將評估安全性和藥物動力學。由於 Fosrenol的生物等效性先前已確定,因此無需進行統計分析即可證明功效;根據505(b)(2)監管途徑,無需進行其他臨床研究即可提交 NDA。該試驗預計將招募60名可評估的參與者。一旦參與者參加試驗,他們將經歷兩週的清除期,以清除系統中目前的磷酸鹽結合劑。參與者最初將以 500 mg OLC每天3次(TID)給藥,然後逐漸滴定至臨床有效劑量,定義為達到 ≤ 5.5 mg/dL血清磷酸鹽範圍所需的劑量。測試的OLC最大劑量為3000毫克/天(1000毫克TID)。

得通路者得天下,沒通路只能陪嫁,
裡裡外外看一遍,保瑞美時堪稱霸!
橫批:一起致富
上聯:一個人走容易走歪
下聯:一群人走慢就是快
致富大道= 長期跟著成功者學習做人,緊緊追隨成效者經營人生,始終選擇與成果者合作方案!
季方案&年方案:https://www.cmoney.tw/app/ItemContent.aspx?id=5115
【免責聲明】
《鬼道》致富APP訂閱者必須完全瞭解,您所支付的訂閱費用是軟體APP的更新維護費用,與社團成員們在同學會和社團內的發文、互相分享、討論沒有任何對價關係。《鬼道》致富APP只是一款模擬台股的資料分析軟體,其中的選股策略及市場分析,僅是彙整部份投資相關書籍邏輯的研究心得。APP提供者並沒有對任何人,做任何真實股市中的買進(或)賣出建議。所有分析資料僅供參考,畢竟模擬與真實之間,必定存在極大的差異性!再者,相同的個股標的、相同的時間點、不同的人因為不同的心理抗壓素質,投資結果會完全不一樣。如果訂閱者自行套用在真實股市中,則必須清楚投資一定有風險,懇請審慎評估自身經濟條件及心理素質,並請自負盈虧,對自己的投資決策行為承擔所有責任!對訂閱者套用在真實股市中的投資決策行為,所導致之直接或間接損失,或因此產生之一切責任,《鬼道》致富APP提供者均不負任何損害賠償及其他法律上的責任。

 發表
發表


 我的網誌
我的網誌



