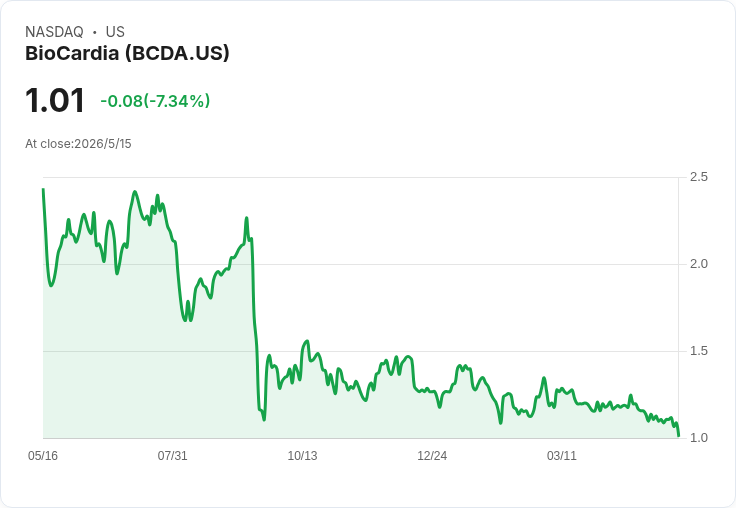
BioCardia獲FDA突破療法認定與Medicare約2萬美元給付、CARDIAMP顯示療效,但現金僅951千美元、HF2試驗與日本申請仍需資金與時間。
BioCardia在2026年第一季財報電話會議交出「臨床+監管」雙利多,但同時暴露資金瓶頸與執行風險。公司宣佈CARDIAMP心衰試驗出現可觀的心功能與生活品質改善,並獲美國FDA授予突破療法(Breakthrough)認定;Medicare亦對該療法擬給付約20,000美元每例,這些進展大幅提升商業化前景的可行性。然而,截至本季末公司帳上現金及約當現金僅951,000美元,顯示短期資金有限,需透過交易或募資支應關鍵試驗與監管申請費用。
背景與資料重點: - CARDIAMP臨床資料:公司表示在接受治療的患者中,心功能與生活品質出現統計顯著的改善,這成為獲得FDA突破認定與臨床推進的基礎。FDA在Q‑sub會議上對療效結果表達「有趣且鼓勵繼續」的態度,促請公司完成正在進行的CardiAMP Heart Failure II(HF2)試驗。 - 美國給付與商業化:Medicare擬提供約20,000美元的給付,若最終落實,將提高醫院與醫師採用的誘因,並為商業化收入建立先期基礎。 - 日本路徑與市場估算:日本藥監(PMDA)對公司提交資料持正面傾向,預計需準備龐大STED檔案、臨床與製造稽核,提交準備約7個月、審查約1年,整體估計約19個月可望取得核准並進入帶給付的上市後研究。日本潛在病人數約30萬名缺血性心衰患者,初期目標市場約2萬名病人,以2萬美元每例估算約4億美元市場機會。 - 財務概況:本季總費用減少46萬美元至230萬美元,主因研發費用下滑;淨損為230萬美元,帳上現金僅951,000美元,但營運現金使用較去年稍增,顯示仍有資金壓力。GuruFocus亦偵測到對BCDA的1項警示訊號,提示投資人留意風險。
深入分析與評論: BioCardia目前處於「高價值但高風險」的典型早期商業化階段。正面因素包含:FDA突破認定(可加速審查與監管互動)、美國給付提案(提升採用動機)以及初步臨床訊號(支援療效主張)。若HF2試驗持續驗證療效並完成日本與美國的註冊路徑,該療法具備顯著的每例營收潛力,能在具體市場中取得商業化回報。
風險與反對觀點(並予以駁斥或說明): - 反對觀點:有意見指出初期市場規模受限(日本首階段目標僅2萬例)、監管與給付仍存在不確定性,且公司現金偏低可能導致執行拖延或需高稀釋性融資。 - 回應與評估:上述疑慮合理且不可忽視;但公司已獲FDA突破認定與Medicare給付估算、PMDA表現出接受資料的傾向,這些有助於降低部分監管與商業化不確定性。關鍵仍是HF2試驗結果、日美正式審核過程與公司能否在短期內完成資金補強。若三項中的任何一項失敗,商業化前景將受重大影響。
未來展望與行動建議: 短期關鍵里程碑包括:HF2試驗的持續入組與正向資料、完成CardiAMP Shonen(日本前市販申請)以及公司籌資或交易以確保試驗與申請能順利推進。對投資人與業界觀察者而言,應密切關注(1)HF2的中期/最終資料公佈,(2)日本提交與PMDA回應時間表,(3)公司資金動向與資本交易條件。公司若能在未來12–24個月內同時交出正向臨床資料與可行的資金方案,則商業化與市場回報的可能性將顯著提升;反之,資金耗盡或試驗失敗將使潛在價值大幅折損。
總結: BioCardia目前握有具吸引力的臨床與監管訊號,但正處於需以資金與臨床成就橋接「實驗室到市場」差距的關鍵階段。投資與合作決策應以接下來HF2進展、日美監管互動與資金策略為核心指標,謹慎評估潛在回報與風險。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌