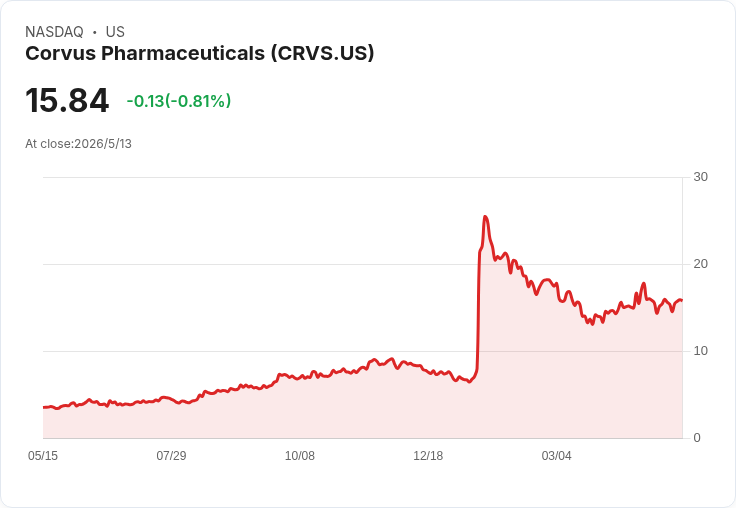
72人一期顯示200mg組EASI75達50%與75%,安全性可接受,市場反應賣壓明顯。
美國生技公司 Corvus Pharmaceuticals(CRVS)公佈針對異位性皮膚炎(濕疹)候選藥 soquelitinib 的第1期最終資料後,股價週四下跌約13%,引發市場熱議。該藥為口服 ITK 抑制劑,目標治療對外用或系統性治療無效的中重度病患。
背景與主要資料: - 該項第1期試驗共納入72名對既有療法未有足夠反應的中重度異位性皮膚炎患者,分成多個劑量佇列評估藥效與安全性。 - 公司指出,在200 mg 劑量的第3與第4佇列中,分別有50%與75%的受試者達到 EASI75(較基線濕疹面積與嚴重度指數減少75%)的療效端點。 - 安全性方面,在分析的四個佇列中,soquelitinib 與安慰劑組均約有42%的患者報告不良事件,均為第1至第2級,且未造成劑量調整或停藥。
深入分析與解讀: 這組資料呈現兩面訊息。一方面,200 mg 高劑量在部分佇列顯示出相當有吸引力的療效,尤其是在治療耐藥患者族群中取得 EASI75,支援 ITK 抑制作為潛在新機制的可行性;另一方面,投資人仍可能因數據規模有限、隊列間差異與對照資料不足而感到失望,導致股價承壓。值得注意的是,第1期試驗主要為劑量與安全探索,並非為了確立療效而設計,樣本數較小且未必具充分統計檢定力。
對替代觀點的回應: - 支持者會強調高劑量組的EASI75資料代表臨床潛力,且不良事件率與安慰劑相當,顯示安全性可控。 - 然而批評者則指出,單靠小規模一期資料難以預測第2期或後續更大規模隨機試驗的結果;隊列間療效波動也提醒須謹慎解讀。綜合來看,正面訊號需由更大規模、對照嚴密的試驗來驗證。
後續展望與行動呼籲: Corvus 已在進行名為 SIERRA1 的第2期試驗,預計納入約200名中重度異位性皮膚炎、作為後線治療的患者,該試驗結果將是檢驗 soquelitinib 真正臨床價值的關鍵。對投資人與臨床界而言,接下來應重點關注:第2期的療效一致性、長期安全資料與與現有標準治療的比較結果。短期內,建議投資者採取謹慎態度,關注公司公佈更完整的資料細節與 SIERRA1 的中期或最終讀出。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌