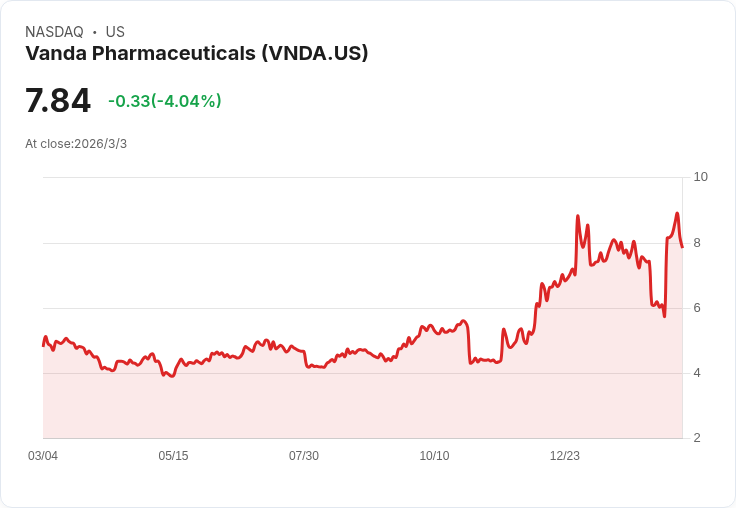
美國FDA同意舉行公聽會,討論Vanda藥廠Hetlioz未能獲批准用於治療時差的原因,此次事件在40年內相當罕見。
在醫藥界的重大進展中,美國食品藥品監督管理局(FDA)最近宣佈將舉行一場公聽會,以審查其對Vanda Pharmaceuticals公司(VNDA)所開發的藥物Hetlioz(tasimelteon)在治療時差方面的拒絕決定。這項決策標誌著自四十多年前以來,FDA首次允許此類公聽會,顯示出該議題的重要性。
Vanda在今年一月提交了申請,希望擴大Hetlioz的適應症,但FDA認為提供的資料未能充分證明其有效性。目前,Hetlioz已被批准用於非24小時睡眠-覺醒障礙及與史密斯-馬根尼斯綜合症相關的夜間睡眠幹擾。
儘管此次公聽會帶來了一絲希望,Vanda股價仍在週二下跌約4%。市場分析師指出,儘管面臨挑戰,Vanda仍有潛力在其他領域取得成功,例如近期Bysanti針對雙相情感障礙和精神分裂症的批准。然而,投資者需謹慎評估風險,尤其是在即將到來的PDUFA期限前夕。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。
文章相關股票

 發表
發表


 我的網誌
我的網誌