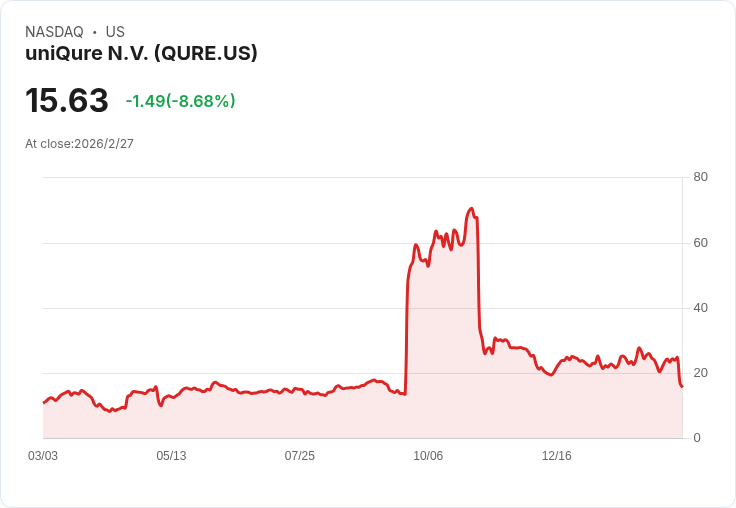
uniQure N.V.在最新財報中透露,為了應對FDA的要求,公司將啟動Phase III隨機雙盲安慰劑試驗,以推進AMT-130治療亨廷頓病。
uniQure N.V.於2025年第四季財報會議上,CEO馬修·卡普斯塔(Matthew Kapusta)強調公司持續致力於基因療法的發展。他提到,AMT-130的Phase I/II研究顯示出顯著的效果,包括75%的疾病程序減緩和60%的功能能力提升。然而,在最近的FDA預BLA會議中,FDA表示目前提交的資料未能支援BLA申請,並建議進行一項Phase III的隨機雙盲安慰劑控制試驗。這使得uniQure必須重新評估其臨床路徑。
首席醫療官瓦利德·阿比薩布(Walid Abi-Saab)指出,AMT-130提供了迄今為止最具說服力的臨床資料,顯示基因療法有潛力改變亨廷頓病的程序。管理層計畫修改Phase I/II協議以納入四年的分析,預期2026年第三季可獲得相關資料。此外,CFO克里斯蒂安·克萊姆特(Christian Klemt)報告稱,2025年收入為1610萬美元,相較於2024年的2710萬美元有所下降,但現金及投資總額達到6.225億美元,顯示公司仍具備良好的財務狀況。
儘管面臨FDA的嚴格要求,uniQure管理層依然對AMT-130的資料充滿信心,並計畫在2026年第二季度與FDA舉行Type B會議,商討Phase III設計選項。在問答環節中,分析師對公司的前景表達了一定的懷疑,尤其是關於多年的安慰劑控制試驗可能帶來的倫理問題和風險。雖然管理層堅持推進其臨床優先事項,但市場對於其美國批准之路的擔憂依然存在。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌